急性心不全治療ガイドライン(2011年改訂版)
Guidelines for Treatment of Acute Heart Failure( JCS 2011)
Guidelines for Treatment of Acute Heart Failure( JCS 2011)
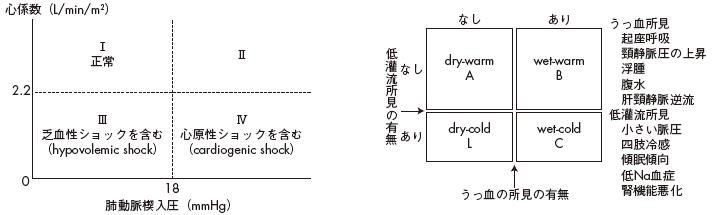
心係数(L/min/m2)Ⅰ正常
肺動脈楔入圧(mmHg)Ⅲ乏血性ショックを含む
(hypovolemic shock)2.2
0 18Ⅳ心原性ショックを含む
(cardiogenic shock)
Ⅱ低灌流所見の有無
なしなしありありうっ血所見 起座呼吸 頸静脈圧の上昇
浮腫 腹水 肝頸静脈逆流低灌流所見
小さい脈圧 四肢冷感 傾眠傾向 低Na血症
うっ血の所見の有無 腎機能悪化
dry-warmA
wet-warmB
dry-coldL
wet-coldC
肺動脈楔入圧(mmHg)Ⅲ乏血性ショックを含む
(hypovolemic shock)2.2
0 18Ⅳ心原性ショックを含む
(cardiogenic shock)
Ⅱ低灌流所見の有無
なしなしありありうっ血所見 起座呼吸 頸静脈圧の上昇
浮腫 腹水 肝頸静脈逆流低灌流所見
小さい脈圧 四肢冷感 傾眠傾向 低Na血症
うっ血の所見の有無 腎機能悪化
dry-warmA
wet-warmB
dry-coldL
wet-coldC
クラスⅠ 心不全の徴候なし
クラスⅡ 軽度~中等度心不全
ラ音聴取領域が全肺野の50%未満
クラスⅢ 重症心不全
肺水腫,ラ音聴取領域が全肺野の50%以上
クラスⅣ 心原性ショック
血圧90mmHg未満,尿量減少,チアノーゼ,
冷たく湿った皮膚,意識障害を伴う
クラスⅡ 軽度~中等度心不全
ラ音聴取領域が全肺野の50%未満
クラスⅢ 重症心不全
肺水腫,ラ音聴取領域が全肺野の50%以上
クラスⅣ 心原性ショック
血圧90mmHg未満,尿量減少,チアノーゼ,
冷たく湿った皮膚,意識障害を伴う
Ⅰ度 心疾患はあるが身体活動に制限はない.
日常的な身体活動では著しい疲労,動悸,呼吸困難あ
るいは狭心痛を生じない.
Ⅱ度 軽度の身体活動の制限がある.安静時には無症状.
日常的な身体活動で疲労,動悸,呼吸困難あるいは狭
心痛を生じる
Ⅲ度 高度な身体活動の制限がある.安静時には無症状.
日常的な身体活動以下の労作で疲労,動悸,呼吸困難
あるいは狭心痛を生じる.
Ⅳ度 心疾患のためいかなる身体活動も制限される.
心不全症状や狭心痛が安静時にも存在する.わずかな
労作でこれらの症状は増悪する.
(付) Ⅱs度:身体活動に軽度制限のある場合
Ⅱm度:身体活動に中等度制限のある場合
日常的な身体活動では著しい疲労,動悸,呼吸困難あ
るいは狭心痛を生じない.
Ⅱ度 軽度の身体活動の制限がある.安静時には無症状.
日常的な身体活動で疲労,動悸,呼吸困難あるいは狭
心痛を生じる
Ⅲ度 高度な身体活動の制限がある.安静時には無症状.
日常的な身体活動以下の労作で疲労,動悸,呼吸困難
あるいは狭心痛を生じる.
Ⅳ度 心疾患のためいかなる身体活動も制限される.
心不全症状や狭心痛が安静時にも存在する.わずかな
労作でこれらの症状は増悪する.
(付) Ⅱs度:身体活動に軽度制限のある場合
Ⅱm度:身体活動に中等度制限のある場合
急性発症の重篤な心不全・心原性ショック
(心筋梗塞・人工心肺離脱困難例・急性心筋炎など)
慢性心不全加療中・基礎心疾患を有する患者の心不全増悪
離脱 強心剤,IABP/PCPS
離脱
回復(-)
回復(-)
適応(+)
回復(+)
回復(+)
適応(-)
緩和ケア 心臓移植適応判定
長期的使用を
目的としたVAD
心臓移植
(心筋梗塞・人工心肺離脱困難例・急性心筋炎など)
慢性心不全加療中・基礎心疾患を有する患者の心不全増悪
離脱 強心剤,IABP/PCPS
離脱
回復(-)
回復(-)
適応(+)
回復(+)
回復(+)
適応(-)
緩和ケア 心臓移植適応判定
長期的使用を
目的としたVAD
心臓移植
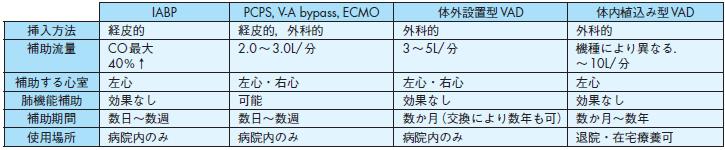
IABP PCPS,V-A bypass,ECMO 体外設置型VAD 体内植込み型VAD
挿入方法経皮的経皮的,外科的外科的外科的
補助流量CO最大
40%↑
2.0~3.0L/分3~5L/分機種により異なる.
~10L/分
補助する心室左心左心・右心左心・右心左心
肺機能補助効果なし可能効果なし効果なし
補助期間数日~数週数日~数週数か月(交換により数年も可) 数か月~数年
使用場所病院内のみ病院内のみ病院内のみ退院・在宅療養可
挿入方法経皮的経皮的,外科的外科的外科的
補助流量CO最大
40%↑
2.0~3.0L/分3~5L/分機種により異なる.
~10L/分
補助する心室左心左心・右心左心・右心左心
肺機能補助効果なし可能効果なし効果なし
補助期間数日~数週数日~数週数か月(交換により数年も可) 数か月~数年
使用場所病院内のみ病院内のみ病院内のみ退院・在宅療養可
① 補助循環の目的と急性重症心不全におけるその位置づけ
機械的補助循環は薬物治療抵抗性の難治性心不全患者に用いる119).大動脈バルーンパンピング(IABP),心肺補助装置(PCPS,V-A
bypass,ECMO),補助人工心臓(VAD)がある.それぞれの特徴について表28に示した.短中期的な補助は人工心肺からの離脱困難例,広範囲
心筋梗塞,血行動態が破綻した急性心筋炎(劇症型心筋炎),重篤な拒絶反応を来たした心臓移植後患者などが対象となり,離脱ないし長期補
助までのブリッジとして用いられる.長期的な補助は心臓移植適応基準に準じた難治性心不全患者(拡張型心筋症,拡張相肥大型心筋症,虚血
性心筋症など)を対象に主に心臓移植までのブリッジ(bridge to transplantation)として用いられる.急性心不全における機械的補助循環の適応
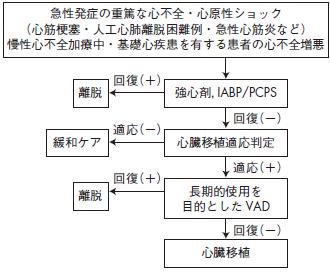
はNYHAクラスⅣ,収縮期血圧90mmHg以下, 心係数2.0L/分/m2以下,肺動脈楔入圧20mmHg以上を目安とする120).図12に補助循環を用いた
際の急性心不全治療アルゴリズムを示した.
②機械的補助循環の種類とそれぞれの適応
1)大動脈内バルーンパンピング(IABP)
大動脈内に挿入したバルーンカテーテルを心臓と同期させ,拡張期にバルーンを膨張し,拡張期圧上昇・冠血流を増大させる.また,収縮期にバ
ルーンを脱気して後負荷軽減効果により,心筋の酸素消費量( 需要)を減少させる.
①適応121)
IABPは簡便な循環補助装置である.内科的治療に抵抗する急性心不全,心原性ショックでまず試みられる(クラスⅠ,レベルB)(表19).また急
性冠症候群における梗塞領域の拡大予防,狭心痛の緩解,切迫梗塞の予防,虚血・低心拍出状態による重症不整脈改善,などに役立つ(クラス
Ⅱa,レベルB)(図9,12).またハイリスクの冠動脈再建術において予防的なIABP使用の有用性も報告されている(クラスⅡa,レベルB)(図9,
12).
非侵襲的に,IABPと同様の働きを期待できる機器として体外設置型カウンターパルセイション機器が開発され,心不全治療への活用が検討され
ている122).
②禁忌
中等度以上の大動脈弁閉鎖不全を合併する患者や,胸部あるいは腹部に大動脈解離,大動脈瘤を有する患者では禁忌である.また,高度の大
動脈粥状硬化病変や下肢閉塞性動脈硬化症を有する患者に対しては慎重に検討する.
③合併症(主なもの)
下肢虚血,出血,バルーン破裂,動脈損傷(動脈解離を含む),コレステロール塞栓症,脊髄動脈虚血による脳神経障害,腹部臓器虚血(腸管虚
血)など.
2)経皮的心肺補助法(PCPS,V-A バイパス,ECMO)
PCPSは遠心ポンプと膜型人工肺を用いた閉鎖回路の人工心肺装置による心肺補助装置である.大腿静脈から挿入した脱血管を介して右房か
ら遠心ポンプにより脱血し,人工肺で酸素化して大腿動脈に送血する.小児のように大腿動静脈が使用できない患者は,開胸により右房,上行大
動脈に直接カニュレーションを行う(V-Abypass).通常1週間程度の運用であるが,数週間にわたる連続運用も可能である.また,呼吸補助として
用いられる場合もある(ECMO).
①適応
心肺停止状態,ないし心原性ショック状態での心肺蘇生(クラスⅠ,レベルB)(表19,20),難治性心不全での呼吸循環補助(クラスⅡ a,レベル
C)(表19,28),開心術後低拍出状態(クラスⅡa,レベルC)(図9),薬剤抵抗性難治性不整脈,重症呼吸不全,などが挙げられる.
②禁忌
高度の閉塞性動脈硬化症.また,中等度以上の大動脈弁逆流症,出血傾向のある患者,最近発症した脳血管障害・頭部外傷患者,薬剤治療
抵抗性の敗血症患者では困難である.
③方法および管理
流量は循環血液量,送血・脱血管のサイズ,位置によって規定される.補助流量2.0L/分以上を目安とし,平均動脈圧60mmHg以上で尿量が確
保できる血圧を保ち,混合静脈血酸素飽和度60ないし70%以上を目標とする.ヘパリンの持続注入を行い,ACTを200秒前後に管理する.ヘパリ
ン起因性血小板減少症(HIT)の患者ではアルガトロバンにて抗凝固療法を行う123).システム内血栓形成,ガス交換能低下や血漿リークが出現す
れば回路を交換する.離脱は補助流量が1.5L/分以下にまで減少できれば,ON/OFFテストを行い,可否を判断する.カテーテル抜去は圧迫止血,
または血管縫合する.
④合併症
送脱血カニューレ挿入部での出血,血管損傷,下肢の血栓症・虚血,後腹膜血腫,神経系合併症,感染症,肺障害などがある.
3)補助人工心臓
最大限の薬物治療を行い,かつIABPやPCPSなどの補助循環治療によっても低心拍出状態から脱せず,臓器循環や末梢組織への十分な酸素
供給が得られない患者であり,かつ除外条件に抵触しない症例が適応となる(クラスⅡ a,レベルB)(表19,20)119).心臓移植適応患者では,
(1)移植待機期間の予測,(2)待機期間中の死亡率,(3)手術のリスク124)-126),を考慮し,適切なタイミングで装着する.入退院の繰返しや薬剤
への抵抗性が高まれば,手術機会を失しないよう留意する.対象患者がカテコラミン依存状態に陥ると6か月生存は50%未満である.早期より
VAD植込み実施施設に患者の病態を照会し,適切なタイミングで対応できるよう留意する127),128).適応患者の社会的・心理的背景についても
ソーシャルワーカーや精神科医にコンサルトする.
右心不全の重症度はLVAD装着の成否を左右する129),130).先行する昇圧薬使用,AST 80IU/L以上,総血清ビリルビン値2mg/dL以上,血清ク
レアチニン値2mg/dL以上はLVAD術後の右心不全の予測因子である(ミシガンスコア)131).心係数2.2L/分/m2以下,右室一回仕事係数
0.25mmHgL/m2以下,血清クレアチニン値1.9mg/dL以上,開胸手術の既往,収縮期血圧96mmHg以下,心エコーにて右室収縮機能の高度低
下,はさらにRVADを必要とする予測因子となる(U-PENNスコア)132).RVADの管理は血栓形成などを起こしやすく,困難を伴う.そのため両心補
助を要した患者においても右室機能の回復後は速やかにRVADを離脱し,LVAD単独の補助に早期に切り替える.左心系の補助を必要としない右
心補助単独の患者は極めてまれである.
【体外設置型補助人工心臓】
体外設置型VADはダイアフラム型の拍動流空気駆動ポンプで,両心補助が可能である.小さな体格の患者でも使用できる.脱血用カニューレ挿
入部位または左房や左室に使い分けられ,いずれも上行大動脈に送血される.
①適応
数か月単位での回復・離脱が見込める心不全患者や,両心補助が必要な患者が適応となる.また,体格が小さいなどの理由で体内植込み型
VADが使用できない患者も心臓移植までのブリッジデバイスとして使用される.
②禁忌
(1)回復が期待できない多臓器不全患者,(2)癌などの予後不良な悪性疾患,(3)予後不良の中枢神経疾患(脳梗塞・脳出血を含む)患者,
(4)治療抵抗性の重篤な感染症,重度の呼吸不全,高度の出血傾向などがある患者は禁忌となる.中等度以上の大動脈弁閉鎖不全症,上行大
動脈高度石灰化の患者への適応も困難である.
③管理
ワルファリンと抗血小板薬を併用して抗凝血療法を行い,プロトロンビン時間(PT-INR)を3.0から4.0程度の範囲に維持する.ポンプチューブの皮
膚挿入部の固定
や消毒を入念に行い,ポンプ部の血栓形成に留意する.装着後も引き続き入院管理を必要とし,原則として外出や退院は許可されない.
④合併症
出血,感染症(ケーブル貫通部,ポンプポケット,敗血症など),脳神経障害(脳梗塞,脳出血など),不整脈,心膜液貯留(タンポナーデ含む),装
置故障,右心不全,溶血,肝・腎・肺などの内臓機能障害(多臓器不全含む),精神障害,他の塞栓症(心筋梗塞など),などに注意する.
【体内植込み型補助人工心臓】
現在用いられる体内植込み型VADは連続流型(遠心,軸流)ポンプで,左室補助目的に用いられる.いずれも左室より脱血し,上行大動脈に送
血する.
①適応
心臓移植適応がある難治性心不全患者で,最大限の薬物治療,ないしはIABP補助によっても低心拍出状態より改善せず,末梢循環への十分
な酸素供給が得られない症例が対象となる.なお,長期在宅治療が可能で,社会復帰が期待できる患者であり,補助人工心臓の限界や併発症を
理解し,家族の理解と支援が得られること.
②禁忌
体外設置型に準じるが,長期在宅治療および社会復帰が行えない場合は適応とならない.
③管理
ワルファリンと抗血小板薬に基づく抗凝血療法を行い,プロトロンビン時間(PT-INR)をデバイスに応じて調整する.駆動ケーブルの皮膚挿入部の
消毒,固定を入念に行い,感染に注意する.在宅療養基準を満たせば,退院・社会復帰することも可能である.体外設置型に比べ高いQOLが期待
できる133),134).
④合併症
体外設置型と同様であるが,他に消化管圧迫による食欲不振や消化管穿孔,それにvon Willbrand因子消費による消化管出血,大動脈閉鎖不
全症の出現などがある.
③補助人工心臓治療の世界の現況
心臓移植までのブリッジ使用だけでなく,心臓移植が高齢や心臓以外の臓器不全,悪性腫瘍,ノンコンプライアンスなどで受けられない難治性心
不全患者に対する恒久的使用(destination therapy)としても用いられている.VAD植込みにより心臓移植が受け入れられない要因が解決されれ
ば移植適応となる患者(bridge to candidacy)や,VAD治療後心機能が回復し離脱できる患者(bridge to recovery),心原性ショックの患者に対
する治療方針決定までのつなぎ(bridge to decision),さらに長期使用が可能なデバイスへのつなぎ(bridge to bridge),など多彩な戦略で使用さ
れている.
米国では植込み型VADの市販後登録(INTERMACS)により詳細なデータの収集・解析が行われており,我が国でも同様の全例登録研究(J-
MACS)が開始された.拍動型から連続流型になり,明らかに生命予後やQOLが向上している135),136).
3 補助循環の種類と適応(IABP,PCPS,人工心臓)
表28 補助循環の種類と特徴
図12 急性心不全患者における機械的補助循環装置の選択と治療体系
クラスⅠ
・ 酸素投与(SaO2>95%,PaO2>80mmHgを維持):レ
ベルC
・ NPPV抵抗性,意識障害,喀痰排出困難な場合の気管内
挿管における人工呼吸管理:レベルC
・循環血液量喪失に対する容量負荷:レベルC
・カテコラミン投与:レベルC
・強心薬併用(カテコラミンとPDE阻害薬):レベルC
・ 薬物治療抵抗例に対する補助循環(IABP,PCPS):レベ
ルC
・心肺停止時のエピネフリン静注:レベルB
・ 心肺停止時のエピネフリン気管内投与(静注量の2~
2.5倍を使用):レベルC
クラスⅡa
・NPPV:レベルA
・ 薬物治療の限界を超えた難治性心不全で回復の可能性あ
るいは心臓移植適応のある患者に対する補助人工心臓:
レベルB
クラスⅢ
・心肺停止時の心腔内注射:レベルC
・ 酸素投与(SaO2>95%,PaO2>80mmHgを維持):レ
ベルC
・ NPPV抵抗性,意識障害,喀痰排出困難な場合の気管内
挿管における人工呼吸管理:レベルC
・循環血液量喪失に対する容量負荷:レベルC
・カテコラミン投与:レベルC
・強心薬併用(カテコラミンとPDE阻害薬):レベルC
・ 薬物治療抵抗例に対する補助循環(IABP,PCPS):レベ
ルC
・心肺停止時のエピネフリン静注:レベルB
・ 心肺停止時のエピネフリン気管内投与(静注量の2~
2.5倍を使用):レベルC
クラスⅡa
・NPPV:レベルA
・ 薬物治療の限界を超えた難治性心不全で回復の可能性あ
るいは心臓移植適応のある患者に対する補助人工心臓:
レベルB
クラスⅢ
・心肺停止時の心腔内注射:レベルC

表19 心原性ショックに対する治療
・身体所見【Killip分類(表3),Nohria-Stevensonプロファイル(図1b)】
・血行動態【Forrester分類(図1a)】
・呼吸管理【酸素療法,NPPV,挿管管理】
・薬物療法【利尿薬,硝酸薬,カルペリチド,強心薬】
・非薬物療法【ECUM,CHDF,IABP,PCPS,VAS】
・体位変換,心臓リハビリテーション
❶早期診断・重症度評価・症状改善・血行動態安定化
集中治療
・身体所見【Nohria-Stevensonプロファイル(図1b)】
・一般検査【胸部X線,血漿BNP,心エコー,心臓核医学検査】
・呼吸管理【酸素療法からの離脱,呼吸補助療法】
・薬物療法【持続静注からの離脱,ACE阻害薬(ARB),β遮断薬,利尿薬】
・非薬物療法【CRT-D,運動療法,和温療法,患者管理・患者教育】
・心臓リハビリテーション
❷薬物療法および非薬物療法の適正化・早期離床
一般病棟
・身体所見【 Nohria-Stevensonプロファイル(図1b)】
・重症度評価【NYHA分類(表2),SAS,6分間歩行,心肺運動負荷試験】
・一般検査【胸部X線,血漿BNP,心エコー,心臓核医学検査】
・薬物療法【ACE阻害薬(ARB),β遮断薬,利尿薬】
・非薬物療法【運動療法,和温療法,患者管理・患者教育】
・心臓リハビリテーション
❸患者教育・生活の質の向上・急性増悪予防
外来治療
死亡
入院死亡
再入院NYHA≦Ⅱ
急性増悪
・血行動態【Forrester分類(図1a)】
・呼吸管理【酸素療法,NPPV,挿管管理】
・薬物療法【利尿薬,硝酸薬,カルペリチド,強心薬】
・非薬物療法【ECUM,CHDF,IABP,PCPS,VAS】
・体位変換,心臓リハビリテーション
❶早期診断・重症度評価・症状改善・血行動態安定化
集中治療
・身体所見【Nohria-Stevensonプロファイル(図1b)】
・一般検査【胸部X線,血漿BNP,心エコー,心臓核医学検査】
・呼吸管理【酸素療法からの離脱,呼吸補助療法】
・薬物療法【持続静注からの離脱,ACE阻害薬(ARB),β遮断薬,利尿薬】
・非薬物療法【CRT-D,運動療法,和温療法,患者管理・患者教育】
・心臓リハビリテーション
❷薬物療法および非薬物療法の適正化・早期離床
一般病棟
・身体所見【 Nohria-Stevensonプロファイル(図1b)】
・重症度評価【NYHA分類(表2),SAS,6分間歩行,心肺運動負荷試験】
・一般検査【胸部X線,血漿BNP,心エコー,心臓核医学検査】
・薬物療法【ACE阻害薬(ARB),β遮断薬,利尿薬】
・非薬物療法【運動療法,和温療法,患者管理・患者教育】
・心臓リハビリテーション
❸患者教育・生活の質の向上・急性増悪予防
外来治療
死亡
入院死亡
再入院NYHA≦Ⅱ
急性増悪
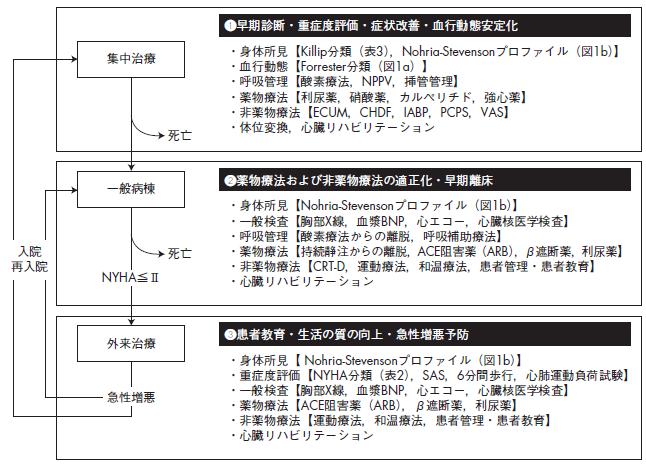
図9 急性心不全治療のフローチャート
呼吸管理
・気道確保:クラスⅠ,レベルC
・酸素投与:クラスⅠ,レベルC
・ 酸素投与のみで酸素化不十分の場合のCPAP,Bilevel PAP
などのNPPV(ただし,表18,19参照):クラスⅠ,レベルA
・ 酸素投与のみで酸素化不十分の場合の気管内挿管(ただ
し,表18,19参照):クラスⅠ,レベルC
原因疾患の治療(可能な場合)
・ 急性心筋梗塞に対する血栓溶解療法/経皮的冠動脈形成
術:クラスⅠ,レベルA
・ 急性大動脈解離に対する外科的治療の適応検討:クラス
Ⅰ,レベルC
・ 徐脈性不整脈に対する一時的ペーシング:クラスⅠ,レ
ベルC
・ 心タンポナーデに対する心膜穿刺ドレナージ:クラスⅠ,
レベルC
・ 急性肺血栓塞栓症の急性期で,ショックや低血圧が遷延
する血行動態が不安定な例に対しての血栓溶解療法:ク
ラスⅠ,レベルC
急性心不全の各病態に応じた薬物治療
・ 硝酸薬舌下,スプレーまたは静脈内投与:クラスⅠ,レ
ベルB
・心肺停止時のエピネフリン静注:クラスⅠ,レベルB
・ 急性肺水腫に対する利尿薬静脈内投与:クラスⅠ,レベ
ルC
・ 著明な高血圧を伴う急性肺水腫におけるニトログリセリ
ン,Ca拮抗薬(ニカルジピンなど):クラスⅠ,レベルC
・ 心原性ショックに対するカテコラミン:クラスⅠ,レベ
ルC
・ 薬物治療で循環動態が改善しない場合の補助循環:クラ
スⅠ,レベルC
・ 救急処置室での初期治療の後,急性冠症候群の治療のた
め速やかにCCUへ搬送:クラスⅠ,レベルC
・モルヒネ静注:クラスⅡb,レベルB
・ 高血圧緊急症時のニフェジピン舌下:クラスⅢ,レベルC
・心肺停止時の心腔内注射:クラスⅢ,レベルC
・気道確保:クラスⅠ,レベルC
・酸素投与:クラスⅠ,レベルC
・ 酸素投与のみで酸素化不十分の場合のCPAP,Bilevel PAP
などのNPPV(ただし,表18,19参照):クラスⅠ,レベルA
・ 酸素投与のみで酸素化不十分の場合の気管内挿管(ただ
し,表18,19参照):クラスⅠ,レベルC
原因疾患の治療(可能な場合)
・ 急性心筋梗塞に対する血栓溶解療法/経皮的冠動脈形成
術:クラスⅠ,レベルA
・ 急性大動脈解離に対する外科的治療の適応検討:クラス
Ⅰ,レベルC
・ 徐脈性不整脈に対する一時的ペーシング:クラスⅠ,レ
ベルC
・ 心タンポナーデに対する心膜穿刺ドレナージ:クラスⅠ,
レベルC
・ 急性肺血栓塞栓症の急性期で,ショックや低血圧が遷延
する血行動態が不安定な例に対しての血栓溶解療法:ク
ラスⅠ,レベルC
急性心不全の各病態に応じた薬物治療
・ 硝酸薬舌下,スプレーまたは静脈内投与:クラスⅠ,レ
ベルB
・心肺停止時のエピネフリン静注:クラスⅠ,レベルB
・ 急性肺水腫に対する利尿薬静脈内投与:クラスⅠ,レベ
ルC
・ 著明な高血圧を伴う急性肺水腫におけるニトログリセリ
ン,Ca拮抗薬(ニカルジピンなど):クラスⅠ,レベルC
・ 心原性ショックに対するカテコラミン:クラスⅠ,レベ
ルC
・ 薬物治療で循環動態が改善しない場合の補助循環:クラ
スⅠ,レベルC
・ 救急処置室での初期治療の後,急性冠症候群の治療のた
め速やかにCCUへ搬送:クラスⅠ,レベルC
・モルヒネ静注:クラスⅡb,レベルB
・ 高血圧緊急症時のニフェジピン舌下:クラスⅢ,レベルC
・心肺停止時の心腔内注射:クラスⅢ,レベルC
表20 救急処置室での初期対応

表2 NYHA(New York Heart Association)分類
表3 Killip分類:急性心筋梗塞における心機能障害の重症度分類


図1a Forresterの分類 図1b Nohria-Stevensonの分類