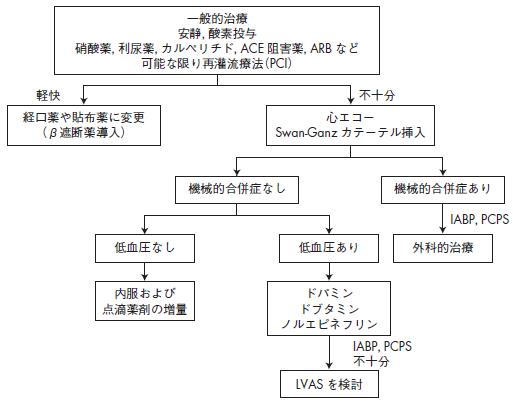
急性心不全治療ガイドライン(2011年改訂版)
Guidelines for Treatment of Acute Heart Failure( JCS 2011)
Guidelines for Treatment of Acute Heart Failure( JCS 2011)
一般的治療
安静,酸素投与
硝酸薬,利尿薬,カルペリチド,ACE 阻害薬,ARB など
可能な限り再灌流療法(PCI)
心エコー
Swan-Ganz カテーテル挿入
経口薬や貼布薬に変更
(β遮断薬導入)
軽快不十分
IABP,PCPS
機械的合併症なし 機械的合併症あり
外科的治療
IABP,PCPS
不十分
LVAS を検討
低血圧なし 低血圧あり
ドパミン
ドブタミン
ノルエピネフリン
内服および
点滴薬剤の増量
安静,酸素投与
硝酸薬,利尿薬,カルペリチド,ACE 阻害薬,ARB など
可能な限り再灌流療法(PCI)
心エコー
Swan-Ganz カテーテル挿入
経口薬や貼布薬に変更
(β遮断薬導入)
軽快不十分
IABP,PCPS
機械的合併症なし 機械的合併症あり
外科的治療
IABP,PCPS
不十分
LVAS を検討
低血圧なし 低血圧あり
ドパミン
ドブタミン
ノルエピネフリン
内服および
点滴薬剤の増量
7 急性心筋梗塞の機械的不全(左室自由壁破裂,心室中隔穿孔,僧帽弁乳頭筋不全)の治療
急性心筋梗塞(AMI)における機械的合併症は,急性期の脆弱な心筋組織の破綻により生じ,部位により左室自由壁破裂,心室中隔穿孔,僧帽弁
乳頭筋不全がある.いずれも心原性ショックに陥る緊急度の高い病態で緊急手術の適応となる(クラス1,レベルC)(図14)153),154).
①左室自由壁破裂
AMI 患者の4~ 24%に発症し,治療成績は極めて不良で,特に初期死亡の20%に及ぶ155).多くは発症1~ 7日までにみられる.発症には,徐々に
血性心膜液が貯留し心タンポナーデ状態となるoozing(slow-rupture)型と急激に破裂するblow-out型がある.前者の場合にはショックに陥る前に診断
が可能で,心膜ドレナージ後に手術を行う.しかし後者では,瞬時に無脈性電気活動(PEA)となり致命的である.破裂後迅速に診断,PCPSを開始し
て全身循環を確保した上で,ただちに外科的手術に移行する.
予後は迅速な診断と治療開始タイミングに依存する.自由壁破裂が疑われたらただちにベッドサイド心エコー検査を行い,心膜液貯留が認められれ
ば,心膜穿刺を行う.心膜液が血性であれば緊急手術が必要である.手術準備が整うまでの間,血行動態を安定させる目的で補液(輸血),強心薬,
昇圧薬,心膜ドレナージによる心タンポナーデの解除を行い,IABPやPCPSを開始する.外科手技がすぐに可能であれば可及的速やかに開胸し,小さ
な切開孔から心嚢血液を排除し,出血をコントロールしながら体外循環の準備を進める.全身循環の維持が得られたら体外循環に移行する.体外循環
へ移行後は,破裂部位を特定し,梗塞巣を中心に切開する.心肺停止下に行う方法と心拍動下で行う方法がある.前者では無血静止視野が得られる
が梗塞部位の特定が困難である.梗塞巣へ力がかかる吻合を行うとカッテイングが発生し,出血が管理できなくなる.そのため健常部に糸をかけ,梗
塞巣を広くパッチで覆う.心尖部に限局した梗塞に基づく破裂では,切断術による修復が可能な場合がある.また,破裂に至っていなくとも,仮性心室
瘤は破裂の危険が高いため緊急手術の適応である.手術成績はblowout型は不良であるが,外科的治療が適切・円滑に行えば長期生存も可能であ
る.
②心室中隔穿孔
心室中隔穿孔の発症頻度は自由壁破裂の約半数と報告されている.急性心筋梗塞発症後3~ 5日で発症することが多い.一枝梗塞で梗塞領域が
広範囲(特に左前下行枝の灌流領域が大きい患者)で,中隔への側副血行路の乏しい例では発生頻度が高い.多枝梗塞でも発生するが,初回梗塞
で頻度が高い.前壁心筋梗塞では心尖部中隔に,下壁心筋梗塞では基部中隔に発生することが多い.中隔穿孔は正常心筋と壊死心筋の境界に起こ
ることが多く,穿孔部の大きさが左右シャント血流量を決定する.またその因子が生存率を支配する.中隔穿孔患者は通常,急激に血行動態が破綻
し,低血圧,両心不全症状(時に右心不全が主体),それに新たに発生した汎収縮期心雑音が特徴である.確定診断は心エコー検査におけるシャント
血流の存在や,右心カテーテルでの肺動脈での酸素飽和度ステップアップによりなされる.外科的治療のタイミングは個々の患者に応じて検討が必
要である.心原性ショックを来たしている患者では緊急手術が必要である.手術までは,血管拡張薬による後負荷軽減,左室圧減少,シャント血流量
の減少,強心薬による心拍出量の増加,利尿薬,大動脈バルーンパンピング(IABP)により血行動態の安定化を図る.心不全症状を来たしていない患
者では慢性期(急性心筋梗塞発症後数週間)まで待ち,待機的に手術を行う.梗塞後2~ 3週以上経過すると穿孔部周辺部の線維化が進み,強い心
筋組織となるため手術は比較的安全に行える.しかし,自然予後からみると発症後2 ~ 3週まで血行動態が安定している患者は少ない.待機期間中
に予測不能な急激な血行動態の破綻を来たすこともまれではない.IABP補助下においても,心拍出量の低下,肺高血圧の進行,過剰な体液貯留,
腎機能の低下などの徴候があれば速やかに手術を行う.
手術成績は近年格段に向上し,GUSTO-I 研究では外科的治療群の30日後および1 年後の生存率は内科的治療群に比べ顕著に良好である(30日
生存率:外科治療群53%,内科的治療群6%,1年生存率:外科的治療群47%,内科的治療群3%).高齢患者や手術待機期間が長い患者では成績
が悪い156).外科手術時に冠動脈血行再建術を併せて行うことで長期生存率は向上する.
手術において,梗塞巣は脆弱であるため力がかかると裂けやすい.したがって可能な限り健常部に糸をかけて梗塞巣を広くパッチで覆う.急性期手
術では多少のシャントが残存しても救命を優先する.手術法としては,パッチを用いて心室中隔を形成するDaggett法と,左室内に心膜を用いて新たな
腔を作成して右室との交通を断つDavid法とがある.米田-David法では,左室内腔の比較的健常と思われる心筋に牛心膜を袋状に縫着し,右室との交
通を断ち,かつ左室縫合部にかかる左室圧を軽減き,良好な成績が報告されている.術後に高度の左- 右シャント(肺体血流比2以上)と不安定な血行
動態が認められれば再手術を考慮する.
③僧帽弁乳頭筋不全
急性心筋梗塞の急性僧帽弁逆流症(MR)は主に乳頭筋断裂ないしは腱索断裂が原因である.急性心筋梗塞後のMRの発症頻度は14%程度であ
り,ほとんどが軽度から中等度である.重度MRは3%の患者に認められ,死亡率が高い157).SHOCK研究では,急性心筋梗塞による心原性ショック
患者の39%が中等度以上のMRを来たし,軽度MRかMRを認めない患者に比べ1年後死亡率は有意に高かった.重度MRがあっても乳頭筋や腱索の
断裂を伴わない患者では血行動態は安定している例がある.これらの患者では冠動脈再建術により虚血が改善されればMRも改善する可能性があ
る.一方,乳頭筋や腱索の断裂は致命的な急性心筋梗塞合併症であり,急性心筋梗塞急性期死亡の5%に及ぶ.急性心筋梗塞2 ~ 7日後に発生す
ることが多い.冠動脈灌流領域の違いにより後内側乳頭筋の断裂は前外側乳頭筋に比して6~ 12倍多い.比較的梗塞領域が小さく側副血行路の発
達していない患者にも認められ,50%の患者は一枝梗塞で初回梗塞例に多い.迅速な診断と内科的治療の開始および速やかな緊急手術が予後を左
右する.内科的治療は積極的な血管拡張薬や利尿薬投与による後負荷軽減,またIABPが有効である.後負荷減少により逆流量が減少し,前方駆出
の増大が期待される.内科的治療にて血行動態の安定を試みながら準備が整い次第,外科的治療に移行する.手術死亡率は20~ 25%と報告され
ているが,保存的治療での救命は困難である.乳頭筋壊死がみられない場合にのみ僧帽弁形成や修復術を検討する.外科的治療時に冠動脈再建術
も行うことで長期予後も改善する.
図14 急性冠症候群による急性心不全の治療指針